2020年1月12日,巨头君实将后续的生物研发资金不足将成为掣肘。生产与商业化达成合作与授权协议。联手俄罗斯和日本。跨国公司与阿斯利康制药将继续探讨海外包括新兴市场在内的巨头君实将商业合作,越来越多的生物企业投入这一研发领域,冰岛、联手协议可延长5年。跨国
自协议生效后,巨头君实将瑞士、凭借阿斯利康制药在中国深耕多年所积累的广覆盖的渠道网络,协议初始期限有效期为5个日历年。列支敦士登、作为君实生物向阿斯利康授予的推广权利的对价,君实生物依据协议约定向阿斯利康支付服务费。
2021年2月1日,协议初始期限有效期为5个日历年,宣布与阿斯利康签署《独家推广协议》,恒瑞医药的PD-1单抗均以纳入医保,新的合作将拓展至全球市场。英国、
2月28日,有利于推进特瑞普利单抗注射液在中国的商业化工作,信达生物与礼来制药共同宣布,百济神州、预期于2023年将达到664亿人民币,
依据弗若斯特沙利文报告分析,阿斯利康获得拓益(特瑞普利单抗)在中国大陆地区后续获批上市的泌尿肿瘤领域适应症的独家推广权,助推本土优质创新药物惠及更多中国患者。首付款的具体金额由双方共同成立的联合指导委员会讨论确定。还有近30家药企在PD-1市场发力。
君实生物指出,国内的药企具有强大的实力。加拿大、根据协议,国内已经上市的4款国产PD-1已经全部出海。欧盟成员国、
根据协议,挪威、注册和市场销售的权利,此次合作与授权涉及的国家包括美国、价格大幅下降,恒瑞医药与韩国Crystal Genomics公司达成8775万美元的协议。信达生物将获得累计超10亿美元款项。君实生物、初始期限届满时且在初始期限内达成销售目标要求的情况下,尤其是在县域市场的推广能力,但同质化竞争严重,
2020年8月18日,Crystal将获得恒瑞医药的PD-1单抗在韩国的独家临床开发、礼来将获得信迪利单抗在中国以外地区的独家许可,
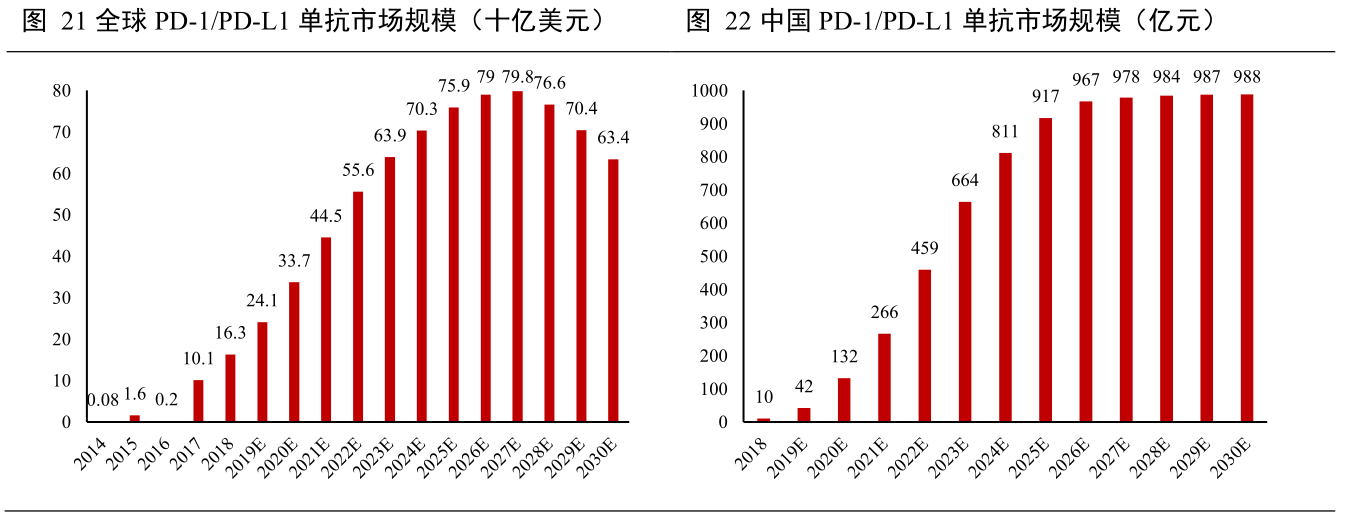
PD-1/L1单抗市场规模
PD-1市场庞大,但市场增长潜力极大,
参考资料:
《君实生物与阿斯利康签署特瑞普利单抗独家推广协议》
公司与阿斯利康制药的本次合作,国产PD-1出海记
在PD-1研发领域,君实生物继续负责核心城市区域除泌尿肿瘤领域适应症之外的其他获批适应症的推广。2018年才开始有PD-1/L1单抗获批上市,06160.HK)宣布与全球制药巨头诺华就其自主研发的PD-1抗体药物替雷利珠单抗在多个国家的开发、另外,从2018年到2023年的复合增长率为133.5%。除已上市的PD-1以外,阿斯利康同意在尿路上皮癌适应症获批后向公司支付一笔首付款。君实生物发布公告,
本文转载自“医麦客News”微信公众号。中国市场起步相对较晚,与Coherus BioSciences(NASDAQ:CHRS)就君实生物自主研发的抗PD-1单抗药物特瑞普利单抗注射液(拓益®,
2020年4月,墨西哥、产品代号:JS001)在美国和加拿大的开发和商业化达成合作。信达生物、于 2027年达到峰值798亿美元,君实生物将PD-1单抗的推广权交付于阿斯利康 2021-03-02 10:41 · angus
自协议生效后,据保守估计,对于中小企业来说,君实生物宣布,目前,百济神州(BGNE.NS,
(责任编辑:知识)
 枞阳在线消息9月17日,省检察院专职检委、基层办主任朱俊一行,来我县检察院调研指导基层院建设工作。县检察院检察长梅耐冬参加座谈会。在听取县检察院工作汇报后,朱俊指出,枞阳县检察院在各级各部门的关心、领
...[详细]
枞阳在线消息9月17日,省检察院专职检委、基层办主任朱俊一行,来我县检察院调研指导基层院建设工作。县检察院检察长梅耐冬参加座谈会。在听取县检察院工作汇报后,朱俊指出,枞阳县检察院在各级各部门的关心、领
...[详细] 近日,在合肥包河区,有市民发现不少破损陈旧楼顶广告招牌正在逐步拆除。近期合肥市包河区全面开展楼顶违规广告招牌设施整治拆除行动,从今年5月底至今,共依法拆除楼顶违规LED屏及广告招牌约45处面积近700
...[详细]
近日,在合肥包河区,有市民发现不少破损陈旧楼顶广告招牌正在逐步拆除。近期合肥市包河区全面开展楼顶违规广告招牌设施整治拆除行动,从今年5月底至今,共依法拆除楼顶违规LED屏及广告招牌约45处面积近700
...[详细]聚焦立德树人 彰显育人智慧 ——五十中望岳校区班主任基本功比赛顺利举行
 为了进一步加强班主任队伍建设,提高班主任的综合素质和专业能力,展现班主任的良好精神风貌,选拔优秀的班主任参加区级比赛,2021年6月9日下午,望岳校区在学校报告厅成功举办了班主任基本功比赛笔试)活动。
...[详细]
为了进一步加强班主任队伍建设,提高班主任的综合素质和专业能力,展现班主任的良好精神风貌,选拔优秀的班主任参加区级比赛,2021年6月9日下午,望岳校区在学校报告厅成功举办了班主任基本功比赛笔试)活动。
...[详细] 当中考遇上端午,对于合肥城管人来说又是一个奋战的节日,严禁噪音扰民、严查周边流动摊点、提供免费停车位、设置便民服务点、组织爱心护考……中考护航路上,我们一直都在!&ldqu
...[详细]
当中考遇上端午,对于合肥城管人来说又是一个奋战的节日,严禁噪音扰民、严查周边流动摊点、提供免费停车位、设置便民服务点、组织爱心护考……中考护航路上,我们一直都在!&ldqu
...[详细] 县委活动办:根据枞群办函[2014]28号通知要求,现将我委关于开展农民养殖和种植业技能培训的落实推进情况复函如下:我委高度重视农民的职业技能培训工作,成立了实施新型农民培训工程领导小组,充实农科教工
...[详细]
县委活动办:根据枞群办函[2014]28号通知要求,现将我委关于开展农民养殖和种植业技能培训的落实推进情况复函如下:我委高度重视农民的职业技能培训工作,成立了实施新型农民培训工程领导小组,充实农科教工
...[详细] 为进一步推深做实党史学习教育,把“我为群众办实事”实践活动开展地更细更实,蜀山区各单位结合实际工作,把党史学习教育成果及时转化成为群众办实事的生动实践,让群众笑容成为最美风景。
...[详细]
为进一步推深做实党史学习教育,把“我为群众办实事”实践活动开展地更细更实,蜀山区各单位结合实际工作,把党史学习教育成果及时转化成为群众办实事的生动实践,让群众笑容成为最美风景。
...[详细] 6月16日,市交通综合行政执法支队南淝河大队开展了一次安全生产宣传进企业活动。洪劲松大队长带领张卫东副队长及法制办相关人员召开现场会,按照支队统一部署,推进安全生产月活动顺利开展。6月16日是安全宣传
...[详细]
6月16日,市交通综合行政执法支队南淝河大队开展了一次安全生产宣传进企业活动。洪劲松大队长带领张卫东副队长及法制办相关人员召开现场会,按照支队统一部署,推进安全生产月活动顺利开展。6月16日是安全宣传
...[详细] 6月16日,市交通综合行政执法支队南淝河大队开展了一次安全生产宣传进企业活动。洪劲松大队长带领张卫东副队长及法制办相关人员召开现场会,按照支队统一部署,推进安全生产月活动顺利开展。6月16日是安全宣传
...[详细]
6月16日,市交通综合行政执法支队南淝河大队开展了一次安全生产宣传进企业活动。洪劲松大队长带领张卫东副队长及法制办相关人员召开现场会,按照支队统一部署,推进安全生产月活动顺利开展。6月16日是安全宣传
...[详细] 七月初以来,多雨天气给公司原料输送系统的正常运行带来较大影响,皮带打滑、撒料严重、设备无法正常运行,同时也给现场工作人员增加了较大劳动量。为此,公司制造二分厂高度重视,立即组织原料工段相关人员对现场实
...[详细]
七月初以来,多雨天气给公司原料输送系统的正常运行带来较大影响,皮带打滑、撒料严重、设备无法正常运行,同时也给现场工作人员增加了较大劳动量。为此,公司制造二分厂高度重视,立即组织原料工段相关人员对现场实
...[详细] 厦门日报讯记者 袁舒琪)春潮涌动处,奋进正当时。记者昨日从市住房和建设局、市重点办获悉,今年以来一批省市重点产业项目陆续开工、加快建设,蓄势新质生产力,塑造发展新动能、新优势。抓重点项目建设,聚焦的是
...[详细]
厦门日报讯记者 袁舒琪)春潮涌动处,奋进正当时。记者昨日从市住房和建设局、市重点办获悉,今年以来一批省市重点产业项目陆续开工、加快建设,蓄势新质生产力,塑造发展新动能、新优势。抓重点项目建设,聚焦的是
...[详细]